Caldo BHI
$ 62.000 + IVA
El Caldo BHI es un medio selectivo para uso general, adecuado para el cultivo de una gran variedad de microorganismos como bacterias, levaduras y hongos, a partir de muestras clínicas filamentosos, a partir de muestras clínicas.
VIDA UTIL: 5 (cinco) Meses
PRESENTACIÓN COMERCIAL:
- Tubo x 3ml
- Tubo x 6 ml
- Tubo x 8 ml
- Tubo x 10 ml
Descripción
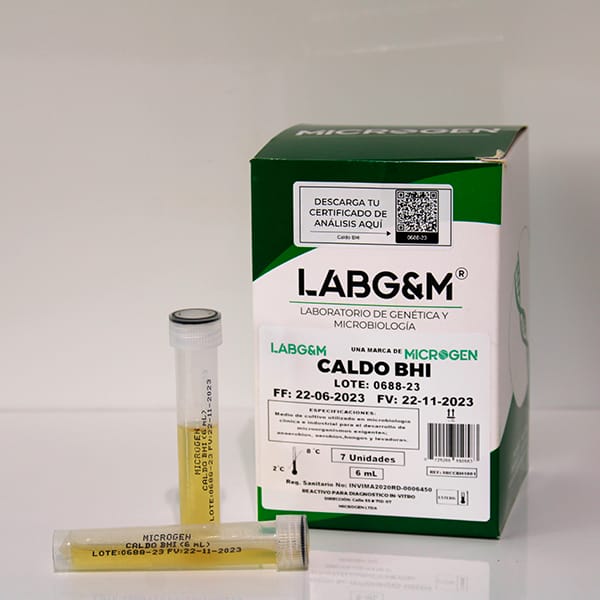
Caldo BHI
APLICACIÓN Y USO DEL CALDO BHI
El Medio Caldo BHI es un medio selectivo para uso general, adecuado para el cultivo de una gran variedad de microorganismos como bacterias, levaduras y hongos, a partir de muestras clínicas.
COMPONENTES DEL CALDO BHI
- Peptona
- Infusión cerebro vacuno
- Infusión corazón vacuno
- Dextrosa
- Cloruro de Sodio
- Fosfato disódico
CONTENIDO DEL ESTUCHE – PRESENTACIÓN DEL CALDO BHI
- Unidad. Caja por 10 tubos.
MATERIALES ADICIONALES
- Indumentaria de trabajo
- Mechero de Bunsen
- Cabina de flujo laminar
- Asas bacteriológicas estériles
- Cepas ATCC
- Equipos y material de Laboratorio.
- Medios de cultivo adicionales, según requerimiento.
METODOLOGÍA
- Principio del método:
Es un medio de cultivo que contiene infusiones de tejidos de cerebro y corazón para el suministro de proteínas y nutrientes para favorecer el crecimiento de microorganismos exigentes y no exigentes.
La infusión de cerebro de ternera, la infusión de corazón vacuno y la peptona, son la fuente de carbono, nitrógeno, y vitaminas.
El medio es adecuado para el cultivo de un amplio número de microorganismos, incluso de patógenos. Esta base de cultivo puede ser enriquecida con sangre o agentes selectivos de crecimiento.
El Medio de Cultivo B.H.I sin suplementar es un medio general de crecimiento para bacterias aeróbicas, y para siembras primarias de hongos y de Actinomycetales, de muestras clínicas y no clínicas.
Con el agregado de 20 Ul de Penicilina y 40 µg/ml de estreptomicina, se utiliza este medio para el aislamiento de hongos patógenos.
- Criterios de desempeño y limitaciones del método:
Medio de cultivo líquido altamente nutritivo que permite la recuperación de toda clase de microorganismos. En su cultivo debe evitarse el crecimiento de flora acompañante.
- Preparación de reactivos:
El medio se encuentra listo para su uso.
- Condiciones de almacenamiento y estabilidad de los reactivos
Una vez recibidos en el laboratorio, almacenar en lugar oscuro y seco a una temperatura de 2 a 8ºC en su embalaje original hasta el momento de uso, evitando la exposición a la luz directa, no debe ser congelado con el fin de preservar el medio.
Antes de inocular los tubos deben estar a temperatura ambiente.
- Espécimen o muestra
El medio puede ser utilizado para muestras clínicas, industriales o investigativas
- Procedimiento:
- Contar con un lugar que tenga normas de asepsia estrictas.
- Para contar con una técnica estéril, realizar todo el procedimiento junto a la llama del mechero y/o en una cabina de flujo laminar.
- Tener asa estéril para la toma de muestra
- Realizar el procedimiento según técnicas de cada laboratorio
- El tiempo, temperatura y condiciones de incubación dependen del microorganismo que se quiera recuperar. (Para uso general, inocular las muestras directamente en el medio e incubar los tubos durante máximo 7 días entre 35–37 °C.
- Luego de la incubación, observar el cultivo, según las características de las colonias determinar los posteriores estudios.
.
CÁLCULO DE LOS RESULTADOS ANALÍTICOS:
CONTROL DE CALIDAD DEL CALDO BHI
- Prueba Macroscópica:
Apariencia: Líquido amarillo pálido.
pH final: 7.4 ± 0.2 (25°C).
Volumen: Según presentación comercial
- Prueba de esterilidad: Se realiza una prueba de esterilidad sometiendo un número representativo del lote a incubación entre 24 y 120 horas, a 35-37°C.
- Prueba de Efectividad: La efectividad del medio se controla mediante el cultivo se cultivan con el siguiente control ATCC:
| Microorganismos | Cepa | Crecimiento |
| Candida albicans | ATCC 60193 | Satisfactorio |
| Streptococcus pneumoniae | ATCC 6305 | Satisfactorio |
| Shigella flexneri | ATCC 12022 | Satisfactorio |
| Sin inocular | Control | Ámbar Claro |
PRECAUCIONES Y ADVERTENCIAS DEL CALDO BHI
- Para uso de diagnóstico in vitro.
- Utilizar el medio de cultivo antes de la fecha de expiración.
- Usar elementos de protección personal durante el uso del producto por la exposición a muestras potencialmente peligrosas
- El desecho del medio de cultivo se debe realizar, según los protocolos implementados por cada institución
TECNOLOGÍA Y EQUIPOS UTILIZADOS:
- Cabina de flujo laminar
- APS One
- Master Clave
- Impresora Linx
- Cuarto frío
BIBLIOGRAFÍA:
- Flores, M., and D. Welch. 1992. Section 6. Mycology: culture media, p.6.7.1-6.7.3. In: H.D. Isenberg (ed.), Clinical microbiology procedures handbook, vol. 1. American Society for Microbiology, Washington, D.C.
- Sutton, D.A. 2003. Specimen collection, transport, and processing: mycology. In: Murray, P. R., E. J. Baron, J.H. Jorgensen, M. A. Pfaller, and R. H. Yolken (ed.). Manual of clinical microbiology, 8th ed. American Society for Microbiology, Washington, D.C.
- Land, G. et al. 1991. Aerobic pathogenic Actinomycetales. In: A. Balows, W.J. Hausler, Jr., K.L. Herrmann, H.D. Isenberg, and H.J. Shadomy (ed.), Manual of clinical microbiology, 5th ed. American Society for Microbiology, Washington, D.C.
- Nash, P., and M.M. Krenz. 1991. Culture media, p. 1226-1288. In : A. Balows, W.J. Hausler, Jr., K.L. Herrmann, H.D. Isenberg, and H.J.